Blog.Kalte Wasserbäder und Möhren
Gesund bleiben durch erfolgreichen Kampf gegen freie Radikale und oxidativen Stress
von Prof. Dr. Werner Siems

Es gibt viele Krankheiten, die multiple Ursachen haben. Welche sind die hauptsächlichen Ursachen von Krankheiten? Mikrobielle Erreger, also Bakterien, Viren, Pilze, Protozoen, Prionen, Parasiten, des weiteren Unfälle in Beruf, Sport, Verkehr, Haushalt, exogene Belastungen der Umwelt wie Strahlen, Chemikalien etc., ernährungsbedingte Schäden, Mangel an Bewegung, psychische Fehlbelastungen oder Schädigungen, toxische Einflüsse wie Alkohol, Rauchen, Drogen, Entzündungen, Autoaggressionen. Und dann gibt es den oxidativen Stress, die Einwirkung von Oxidanzien und darunter häufig von so genannten freien Radikalen.
Was sind freie Radikale?
Als freie Radikale bezeichnet man in der Chemie Atome oder Moleküle mit mindestens einem ungepaarten Valenzelektron.
Die meisten freien Radikale sind besonders reaktionsfreudig. Freie Radikale werden graphisch mit einem „Punkt“ dargestellt, der das ungepaarte Elektron symbolisiert, zum Beispiel Hydroxylradikal (HO•). Radikale sind meist sehr reaktionsfreudig. Warum ist das so?
Aus einer Verbindung wird ein Elektron „herausgerissen“, um in dem jeweiligen Atom oder der jeweiligen Verbindung wieder ein komplettes Elektronenpaar zu bilden. Also: Aus irgendeiner Substanz wird ein einzelnes Elektron „herausgerissen“. In diesem Zuge resultiert eine radikalische Kettenreaktion. Und es kommt zur Schädigung von Atomen oder Molekülen, zur Oxidation von Lipiden, Proteinen, Kohlenhydraten oder Nukleinsäuren. Beim Entreißen von Elektronen entsteht immer wieder ein neues Radikal. Es kommt somit zu Radikal-Kettenreaktionen.
Radikale, etwa Sauerstoff-Radikale, spielen bei einer Vielzahl biologischer Prozesse eine wichtige Rolle, können auch Zellschäden hervorrufen, die unter anderem zur Entstehung von Krebserkrankungen beitragen können. Wir haben dies seit fast dreißig Jahren untersucht (Grune et al. 1994, Milkovic et al. 2014).
Auch für die Entstehung der Arteriosklerose, der Alzheimerschen Krankheit, der Leberschädigung durch Alkohol und des Lungenemphysems durch Tabakrauch wird der durch freie Radikale vermittelten Oxidation verschiedener Stoffe eine bedeutsame Rolle zugeschrieben. In der schematischen Abbildung werden verschiedene Krankheiten aufgezeigt, die definitiv mit oxidativem Stress verbunden sind, ja man kann sagen, durch oxidativen Stress verursacht werden. Der Terminus oxidativer Stress wurde durch den deutschen Arzt und Biochemiker Helmut Sies geprägt. (Sies 1986, Sies 2020)

Es gibt im Ablauf eines oxidativen Stress verschiedene „Signalwege“. Unter den intrazellulären Signalwegen, die durch freie Radikale aktiviert werden, ist der NF-κB-Signalweg einer der wichtigsten. NF-κB kann durch die Bindung an bestimmte regulatorische Abschnitte der DNA die Transkription abhängiger Gene beeinflussen, führt z.B. über TNF-α und über IL-1β zur vermehrten Bildung von Prostaglandin-E2.
Dieser Faktor ist vor allem bei der Regulation der Immunantwort, der Zellproliferation, der Entzündungsreaktionen und der Apoptose von großer Bedeutung.
Welche Auswirkungen haben freie Radikale auf den menschlichen und dem Organismus?
o2-Radikale spielen auch eine wichtige Rolle bei der Alterung von Geweben und von Organismen. Die Theorie der freien Radikale des Alterns besagt, dass viele der Veränderungen, die mit dem Altern unseres Körpers einhergehen, durch freie Radikale verursacht werden. Schäden an DNA und andere Veränderungen werden freien Radikalen zugeschrieben. Mit der Zeit akkumuliert sich dieser Schaden und lässt uns altern.
Aus biologischer Sicht gehören freie Radikale häufig zu den Playern des systemischen Prozesses, der als Entzündung bezeichnet wird. Entzündung ist verbunden mit Rötung, Erwärmung, Schwellung, Schmerz, Funktionsreduktion von Zellen, Geweben und von Organen.
Darüber hinaus und möglicherweise noch schwerwiegender, kann eine Entzündung der Entstehung schwerwiegender innerer Erkrankungen vorausgehen, einschließlich Diabetes, Herz-Kreislauf-Erkrankungen, Autoimmunerkrankungen und hormonellen Ungleichgewichten. Freie Radikale sind häufig das Resultat bestimmter Umweltgifte, mit denen Menschen regelmäßig in Kontakt kommen. Dazu zählen Smog, Autoabgase, Luftverschmutzung, aber auch Pestizide und Chemikalien in Haushaltsreinigern und Farben. Auch Lebensmittel und Getränke können erhöhte Mengen von Sauerstoffradikalen beinhalten, vor allem verarbeitete und konservierte Produkte, Zigaretten, Alkohol, Medikamente und Produkte mit hohem Zuckergehalt. (Siems et al. 2005)
Wenn Menschen altern, können sie anfälliger für Störungen und gesundheitliche Probleme sein. Sind zu hohe Mengen an freien Radikalen vorhanden, kann sich dieser Prozess verschlimmern. Eine wachsende Anzahl abnormaler Substanzen kann zu systembedingten Schäden und vorzeitigem Altern führen, was zu unerwünschten Veränderungen des Phänotypus und zahlreichen Krankheiten beiträgt. (Gil et al. 2006, Siems & Voss 2006)
Zufuhr und Bildung von Antioxidantien ist eine der besten Maßnahmen, um freie Radikale zu entgiften. Antioxidantien sind Stoffe, die in zahlreichen gesunden Lebensmitteln enthalten sind. Sie haben die Fähigkeit, den Entzündungsprozess zu drosseln oder in bestimmten Fällen umzukehren. Antioxidantien finden sich in verschiedenen Obst- und Gemüsearten (insbesondere in Trauben, Beeren, Spinat, Grünkohl, Melonen, Karotten, Tomaten und Paprika), sowie manchen Kräutern und Gewürzen (Zimt, Kurkuma, Rosmarin, Oregano und Ingwer) und sind in bestimmten ätherischen Ölen enthalten. Auch Nüsse, Rotwein, Kakao, und grüner Tee stellen gute Quellen dar.
Darüber hinaus sollte die Exposition ("das Ausgesetzsein") gegenüber gefährlichen Schadstoffen beschränkt werden. Zu den bedenklichen Substanzen zählen Pestizide, Dioxine, Methan, Ozon, Lösungsmittel und Schwermetalle. Auch die Verwendung bestimmter Kosmetikprodukte kann ein Risiko darstellen, da diese Produkte häufig über erhöhte Mengen an freien Radikalen verfügen. Menschen, die Berufe ausüben, in denen sie hoher Strahlenbelastung ausgesetzt sind, gelten ebenfalls als gefährdet.
Schlechte Gewohnheiten können sich ebenfalls ungünstig auf die oxidative Belastung auswirken, weswegen auf Genussmittel wie Alkohol und Nikotin entweder ganz verzichtet oder diese signifikant reduziert werden sollten. Vergessen werden soll nicht der Stresslevel. Übermäßige systemische Konzentrationen von Stresshormonen wie Adrenalin und Cortisol können die Produktion verschiedener freier Radikale stimulieren. Nicht zuletzt sollte die Einnahme von Medikamenten betrachtet werden, da einige davon freie Radikalte enthalten oder die Produktion dieser stimulieren. Dazu zählen etwa Antibiotika, Zytostatika oder Hormonpräparate.
Wer bildet die „freien Radikale“?
Am meisten offenbar die Mitochondrien, die Kraftwerke der Zellen, in der Atmungskette (AK) werden freie Radikale gebildet. Normalerweise werden 3% des Durchstroms durch die AK zu o2-Radikalen, bei entkoppelter AK noch mehr. Das ist sehr viel. Bei 75 Bio Zellen mit jeweils mehreren Mitochondrien und einem Sauerstoffverbrauch von 0,3 l pro Minute ist man bei 18 l Sauerstoffverbrauch pro Stunde. Das sind 432 l pro Tag. Davon 3% sind 13 „Liter“ Sauerstoff-Radikale pro Tag und Organismus (bezogen auf einen erwachsenen Organismus).
Dreizehn „Liter“ Sauerstoff-Radikale vernichten einen Organismus, wenn sie nicht entgiftet werden. Und das sind bei weitem noch nicht alle o2-Radikale; in anderen Zellorganellen entstehen ja noch weitere o2-Radikale.
Wo entstehen noch o2-Radikale?
In hypoxischen (unter Sauerstoffmangel leidenden) Regionen, beim Purinabbau (durch die Xanthinoxidase, XO), beim Abbau von Medikamenten, beim Alkoholabbau (vor allem in der Leber), Im Immunsystem, Bei allen Stressreaktionen, beim Abbau von Adrenalin, entstehen massenhaft o2-Radikale. (Siems et al. 1998)
Auf das Gleichgewicht kommt es an! Die Zellen besitzen spezifische Kontrollsysteme, die sowohl die Radikalproduktion als auch die antioxidative Abwehr regulieren. So fungiert zum Beispiel das Protein Keap als Messsystem für den oxidativen Stress in der Zelle. Bei einem Zuviel an Radikalen wird über das Keap-System der Transkriptionsfaktor Nrf2 aktiviert, was die Zelle dann zur verstärkten Produktion von antioxidativen Enzymen wie Katalase und Hämoxygenase I anregt.
Es geht um das Gleichgewicht zwischen Freien Radikalen und Prooxidanzien auf der einen Seite und primären sowie sekundären antioxidativen Schutzsystemen auf der anderen Seite. Das nächste Schema zeigt Komponenten dieses Gleichgewichts auf.
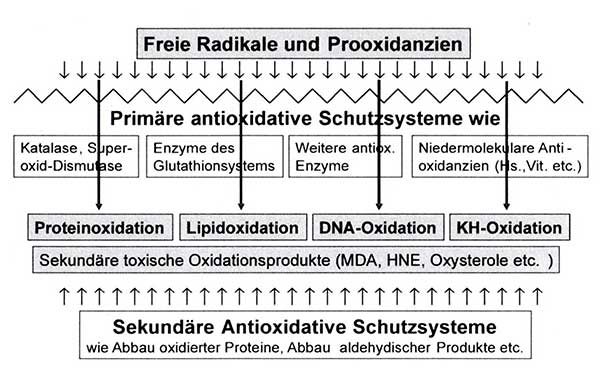
Zu den sekundären antioxidativen Schutzsystemen gehören der Abbau aldehydischer Produkte der Lipidperoxidation, wie z.B. von 4-Hydroxy-nonenal oder von Malondialdehyd, und der Abbau oxidativ modifizierter Proteine durch das proteasomale System (Schaur et al. 2015, Gueraud et al. 2010, Negre-Salvayre et al. 2010, Spickett et al. 2010, Castro et al. 2017).
Antioxidantien sind aufgrund ihrer molekularen Struktur, die sie besonders leicht oxidierbar macht, bevorzugte Reaktionspartner für Radikale. Somit kann man mit großen Mengen an Antioxidantien die Oxidation körpereigener Moleküle teilweise reduzieren.
Die gesteigerte exogene Zufuhr von Antioxidantien über Nahrungszusatzstoffe kann aber unter anderem dazu führen, dass im Körper selbst Antioxidantien in geringerem Maße gebildet werden. Dieser Regelkreis ist einer von vielen Gründen, warum eine reine antioxidative Therapie (mit Vitaminen) mitunter nicht protektiv wirkt. Schema: der antioxidative Schutz (Siems et al. 1998)
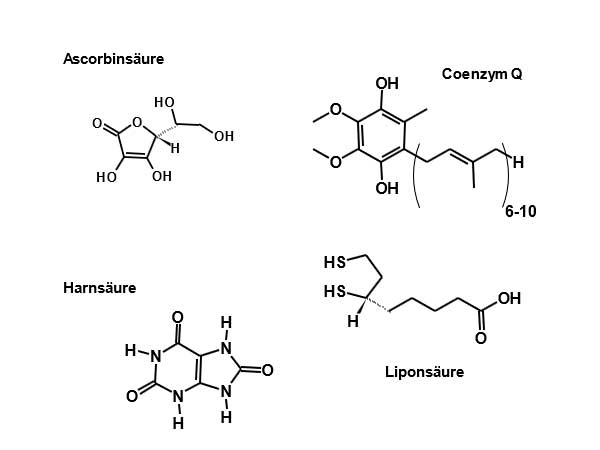
Wir haben Enzyme, die Oxidanzien beseitigen können: Katalase, Superoxid-Dismutase, Glutathionperoxidase, Glutathionreduktase. Und es gibt viele niedermolekulare Antioxidanzien, z.B. Ascorbinsäure, Coenzym Q, Harnsäure, Liponsäure.

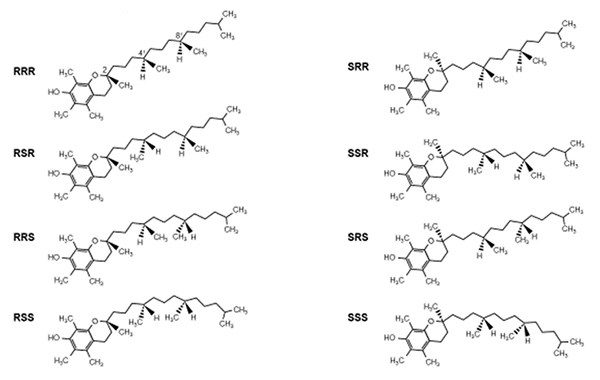
Es gibt die Tocopherole und Tocotrienole, acht Verbindungen, die man zum Vitamin E zusammenfasst.
Und es gibt eine Vielzahl weiterer Verbindungen, die in der Lage sind Oxidanzien bzw. Radikale zu entgiften.
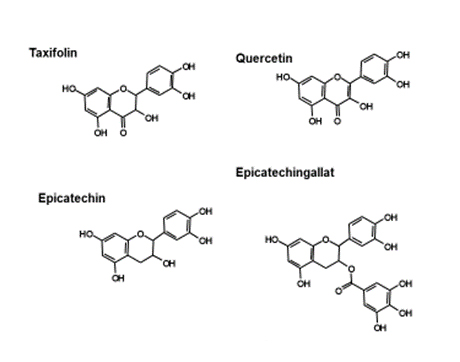
Diese Antioxidanzien, z. T. hydrophil, z. T. hydrophob, haben enge Wechselbeziehungen, sie stabilisieren sich gewissermaßen gegenseitig und ergänzen bzw. ersetzen sich sogar. Im Rahmen dieses antioxidativen Systems spielt das Tripeptid Glutathion, das wichtigste hydrophile zelluläre Antioxidanz, eine zentrale Rolle. Es schützt Proteine vor radikalischem Angriff und regeneriert sich über die Glutathionreduktase immer wieder selbst.
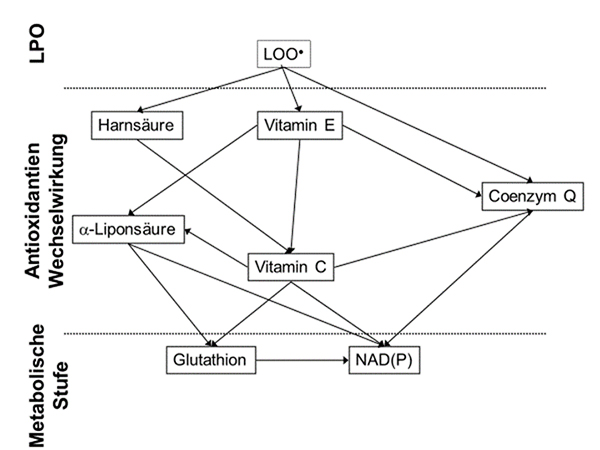
Glutathion und Vitamin E spielen eine zentrale Rolle im antioxidativem Netzwerk.
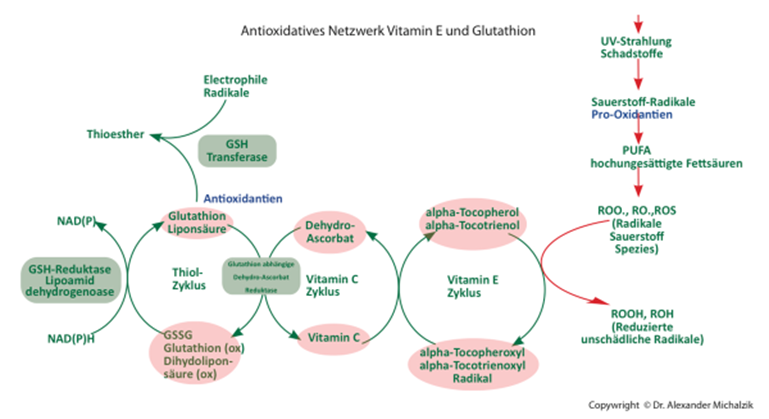
Antioxidanzien-Mangelzustände korrelieren mit Leistungsabfall, Morbidität und Mortalität. Eine ausreichend hohe Antioxidanzien-Zufuhr ist sinnvoll, wenn das Gleichgewicht erheblich gestört ist. Dies kann bei vielen Menschen nicht nur mittels ausgewogener Kost mit ausreichend Früchten und Gemüse erreicht werden. Dennoch: Die meisten Antioxidanzien werden uns durch Obst und Gemüse geliefert.

Obst und Gemüse als beste Lieferanten von Antioxidanzien.

Verschiedene Verbindungen aus Ingwer stärken Immunkräfte unseres Körpers.

Omega 3-Fettsäuren können auch in Eiern angereichert werden.

Flavonoide im grünen Tee und in Rotwein. Nahrungsergänzung in natürlicher Form.
Welche sind die wirksamsten Antioxidanzien?
- Bestandteile von Obst und Gemüse
- Ich bilde selbst antioxidative Schutzenzyme
- Und man kann auch niedermolekulare Antioxidanzien bilden
- Sekundär: es gibt Stoffwechselwege für die Beseitigung oxidativ modifizierter Proteine und Wege für die Beseitigung von Aldehyden
Wichtig sind in besonderem Maße die Vitamine A, C und E
Die Vitamine A und E sind lipophil. Das Vitamin C ist hydrophil. Das Vitamin A ist bedeutsam für den Sehvorgang und für die Ablesung von Genabschnitten. Das Vitamin C ist essentiell für das Immunsystem, aber auch für die Stärkung der verschiedenen Arten von Bindegeweben. Vitamin E ist wichtig für die Membranen, die Blutgefäß-Protektion und die Sexualfunktion. Alle diese Vitamine bekämpfen oxidativen Stress. (Sommerburg et al. 2013)
Man erzeugt viele Antioxidanzien durch Bewegung und nach regelmäßigen hydrotherapeutischen Kaltreizen. Das ist die Antwort auf eine hohe Bildung von o2-Radikalen bei der Muskel-Kontraktion und durch das bei den Kaltreizen auftretende muscle shivering. In besonders starkem Maße erhöht sich die intrazelluläre Konzentration des wohl bedeutendsten hydrophilen Antioxidanz, das man Glutathion nennt (GSH). Es ist das Tripeptid, gamma-Glutamyl-Cysteinyl-Glycin. (Siems et al. 1999)

Dr. Ralf Maas promovierte über biochemische und immunologische Mechanismen im Organismus bei den so genannten Winterschwimmern oder Eisbadern.
Regelmäßige Kaltreize tragen offenbar zur Aktivierung der Killerzellen und anderer anticancerogener Mechanismen (z.B. Stimulierung des Glutathionsystems) bei. Man kann ähnliche biochemische und immunologische Anpassungen aber auch mit Hilfe milder dosierter Kaltreize erreichen. Entscheidend ist nur, dass sie regelmäßig und wiederholend durchgeführt werden.

Quellen- und Literaturhinweise:
Brenke R, Siems W:
Das Buch vom Winterschwimmen. Husum-Verlag, Husum, 1996.
Castro, J.P., T. Jung, T. Grune, W. Siems:
4-Hydroxynonenal (HNE) modified proteins in metabolic diseases. Free Rad. Biol. Medicine (2017).
Gil, L., W. Siems, B. Mazurek, J. Gross, P. Voss, T. Grune:
Age-associated analysis of oxidative stress parameters in human plasma and erythrocytes. Free Radical Res. 40(5), 495-505 (2006).
Grune, T., W. Siems, H. Zollner, H. Esterbauer:
Cancer Research 54, 5231-5235 (1994).
Gueraud, F., M. Atalay, N. Bresgen, A. Dipak Gasparovic, P.M. Eckl, L. Huc, I. Jouanin, W.G. Siems, K. Uchida:
Chemistry and biochemistry of lipid peroxidation. Free Rad Res 2010 Oct. 44 (10): 1098-1124.
Milkovic, L, W. Siems, R. Siems, N. Zarkovic:
Oxidative stress and antioxidants in carcinogenesis and integrative therapy of cancer. Current Pharmaceut. Design 20, 6529-6542 (2014).
Negre-Salvayre, A, N. Auge, V. Ayala, H. Basaga, J. Boada, R. Brenke, S. Chapple, G. Cohen, J. Feher, T. Grune, G. Lengyel, G. Mann, R. Pamplona, G. Poli, M. Portero-Otin, Y. Riahi, R. Salvayre, S. Sasson, J. Serrano, O. Shamni, W. Siems, R. Siow, I. Wiswedel, K. Zarkovic, N. Zarkovic:
Pathological aspects of lipid peroxidation. Free Rad Res 2010 Oct. 44 (10): 1125-1171.
Schaur, R.J., W. Siems, N. Bresgen, P.M. Eckl:
4-Hydroxynonenal – a bioactive lipid peroxidation product. Biomolecules 2015, 5, 2247-2337;doi:10.3390/biom5042247
Sies, H.:
Biochemistry of oxidative stress. Angew. Chemie 25 (12), 1058-1071 (1986).
Sies, H.:
Oxidative Stress: Concept and Some Practical Aspects. Antioxidants 9(9), 852 (2020).
Siems, W.G., R. Brenke, O. Sommerburg, T. Grune:
Improved antioxidative protection in winter-swimmers. QJM (Quaterly J. Medicine) 92, 193-198, 1999.
Siems W., K. Krämer, T. Grune:
Oxidativer Stress und Pharmaka. Govi-Verlag Pharmazeutischer Verlag, Eschborn 2005.
Siems, W.G., F.J.G.M. van Kuijk, R. Maass, R. Brenke:
Uric acid and glutathione levels during short-term whole body cold exposure. Free Radicals Biol. & Medicine 16, 299-305 (1994).
Siems, W.G., O. Sommerburg, H. Mayer, T. Grune:
Die wichtigsten Radikalquellen im menschlichen Organismus. Pharmazeut. Z. 143, 1515-1527 (1998).
Siems, W., P. Voss:
Clinical oxidation parameters of aging. Free Radical Research 40(12), 1339-1349 (2006).
Sommerburg, O., W Siems, K Kraemer:
Carotenoids and Vitamin A in Translational Medicine (A volume in the Series Oxidative Stress and Disease) CRC Press Taylor & Francis, Boca Raton, FL, Boston, MA, USA, 2013
Spickett, C.M., I. Wiswedel, W.G. Siems, K. Zarkovic, N. Zarkovic:
Advances in methods for the determination of biologically relevant lipid peroxidation products. Free Rad Res 2010 Oct. 44 (10): 1172-1202.








